1)Em uma reação, qual a função do complexo ativado:
2)Por que o catalisador altera velocidade de uma reação?
3)(UnB) Assinale as opções corretas:
01)O catalisador afeta a velocidade de uma reação porque aumenta o número de moléculas com energia cinética maior ou igual à energia de ativação da reação.
02)A temperatura afeta a velocidade de uma reação porque muda a energia de ativação da reação.
03)A concentração dos reagentes afeta a velocidade de uma reação porque há alteração no número de colisões efetivas.
04)Uma reação ocorre quando há colisão efetiva entre as moléculas reagentes, numa orientação apropriada.
4) Na coluna I estão relacionadas transformações e, na coluna II, os principais fatores que alteram a velocidade dessas transformações.
COLUNA I
- A transformação do leite em iogurte é rápida quando aquecida.
- Um comprimido efervescente reage mais rapidamente quando dissolvido em água do que acondicionado em lugares úmidos.
- Grânulos de Mg reagem com HCl mais rapidamente do que em lâminas.
- A transformação do açúcar, contido na uva, em etanol ocorre mais rapidamente na presença de microorganismo.
COLUNA II
( ) superfície de contato
( ) temperatura
( ) catalisador
( ) concentração dos reagentes
Relacionando-se as duas colunas obtêm-se, de cima para baixo, os números na seqüência:
a) 2, 1, 4, 3 b) 2, 3, 4, 1 c) 3, 1, 4, 2 d) 3, 1, 2, 4 e) 4, 3, 1, 2
5)No diagrama a seguir estão representados os caminho de uma reação na presença e na ausência de um catalisador. Com base neste diagrama, é correto afirmar que:
a) A curva II refere-se à reação catalisada e a curva I refere-se à reação não catalisada.
b) Se a reação se processar pelo caminho II, ela será, mais rápida.
c) A adição de um catalisador à reação diminui seu valor de Δ
d) O complexo ativado da curva I apresenta a mesma energia do complexo ativado da curva II.
e) A adição do catalisador transforma a reação endotérmica em exotérmica.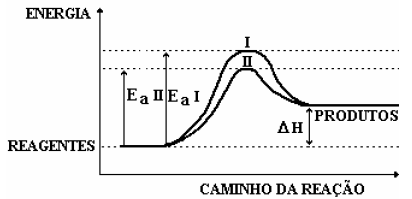
6)O carvão é um combustível constituído de uma mistura de compostos ricos em carbono. A situação em que a forma de apresentação do combustível, do comburente e a temperatura utilizada favorecerão a combustão do carbono com maior velocidade é:
a) Combustível - carvão em pedaços; Comburente – ar atmosférico; Temperatura 0°C.
b) Combustível - carvão pulverizado; Comburente – ar atmosférico; Temperatura 30°C.
c) Combustível - carvão em pedaços; Comburente - oxigênio puro; Temperatura 20°C.
d) Combustível - carvão pulverizado; Comburente - oxigênio puro; Temperatura 100°C.
e) Combustível - carvão em pedaços; Comburente - oxigênio liquefeito; Temperatura 50°
7)Observa-se que a velocidade de reação é maior quando um comprimido efervescente, usado no combate à azia, é colocado:
a) inteiro, em água que está à temperatura de 6°C.
b) pulverizado, em água que está à temperatura de 45°C.
c) inteiro, em água que está à temperatura de 45°C.
d) pulverizado, em água que está à temperatura de 6°C.
e) inteiro, em água que está à temperatura de 25°C.
-
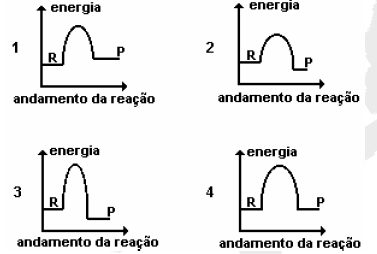
8)Reações químicas ocorrem, geralmente, como resultado de colisões entre partículas reagentes. Toda reação requer um certo mínimo de energia, denominada energia de ativação. Os gráficos a seguir representam diferentes reações químicas, sendo R = reagente e P = produto. Aquele que representa um processo químico exotérmico de maior energia de ativação é o de número: Explique.
- 9)O gráfico a seguir refere-se ao diagrama energético de uma reação química reagentes→produtos), onde se vêem destacados dois caminhos de reação: Após uma analise das entalpias dos reagentes, dos produtos e dos valores a, b, c e d, podemos afirmar que:
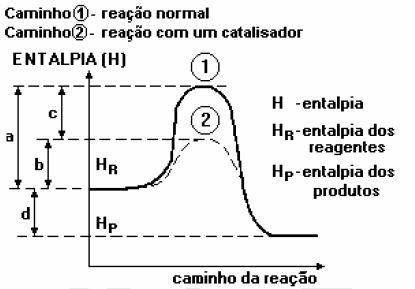
- a) reação é endotérmica e a presença do catalisador diminuiu o ΔH de a para b.
- b) reação é endotérmica e a representa o ΔH com a presença do catalisador.
- c) reação é exotérmica e a energia de ativação, sem a presença do catalisador, é representada por c.
- d) presença do catalisador diminuiu o ΔH da reação representada por c.
- e) presença do catalisador diminuiu a energia de ativação de a para b e mantém constante o ΔH da reação representada por d.
-
- 10)Para responder à questão, julgue as afirmativas abaixo.
- Uma reação com energia de ativação 40 kJ é mais lenta que uma outra reação que apresenta energia de ativação igual a 130 kJ.
- A adição de um catalisador a uma reação química proporciona um novo "caminho" de reação, no qual a energia de ativação é diminuída.
3. Um aumento de temperatura geralmente provoca um aumento na energia de ativação da reação.
4.A associação dos reagentes com energia igual à energia de ativação constitui o complexo ativado.